★主な変異を一度に検査
肥満細胞腫(MCT)および消化管間質腫瘍(GIST)において、c-kit遺伝子に機能獲得性の変異を有する腫瘍に対しては、分子標的治療薬であるイマチニブ(グリベック)やトセラニブ(パラディア)が著効する可能性が高いことが報告されています。
イマチニブによる治療効果と関連があるとされるc-kit遺伝子の変異は、KITタンパクの膜近傍領域に相当する部位で起こるInternal Tandem Duplication(ITD)変異などの複数が知られています(下図)。c-kit遺伝子変異検査ではこれらを一度に検査し、効果予測に有用な変異情報を取得します。
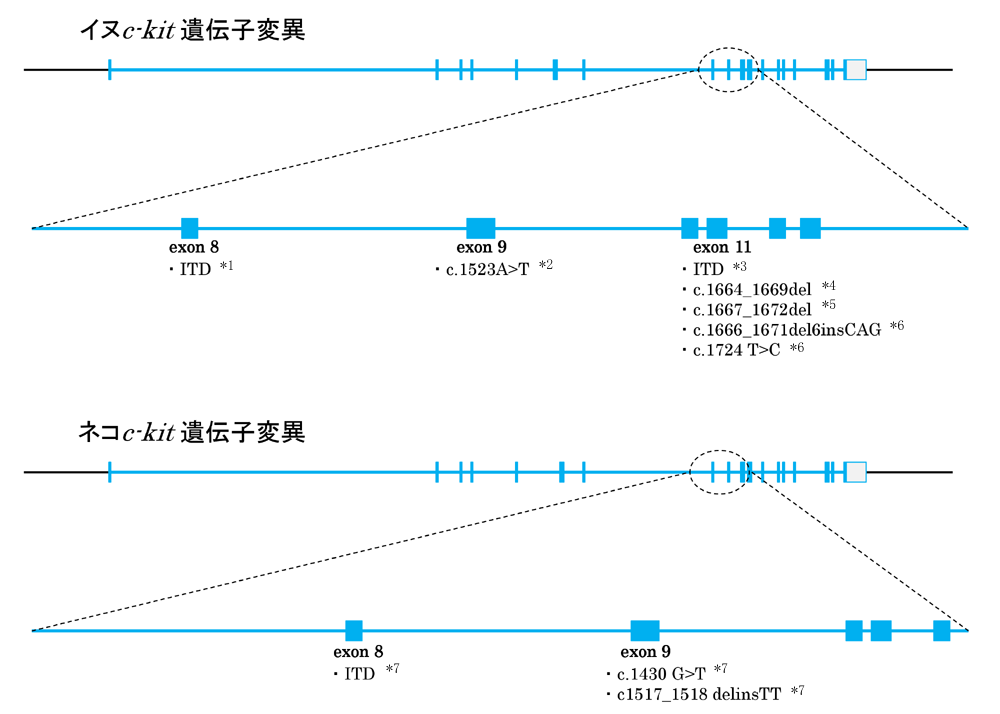
- 本検査で解析する変異部位を図示しています。MCTやGISTで確認されている変異のすべてを示すものではありません。
- 遺伝子変異の記載は一部を除きHuman Genome Variation Societyの記述方法に準じています。
- 上記変異を有する腫瘍であってもイマチニブ等に対して耐性を示す場合が、また、上記変異がない腫瘍でもイマチニブ等による効果を示す場合があります。
- 2016年8月現在の検査情報です。解析する変異部位は実績や新しいエビデンスなどにより変更する場合があります。
*参考文献
- Kobayashi, M., Bonkobara,M. et al. (2012) : Vet J. 193, 264-267.
- Yamada, O., Bonkobara,M. et al. (2011) : Vet Immunol Immunopathol. 142, 101-106.
- Isotani, M., Bonkobara,M. et al. (2008) : J Vet Intern Med. 22, 985-988.
- Letard, S., Dubreuil, P. et al. (2008) : Mol Cancer Res. 6, 1137-1145.
- Kobayashi, M., Bonkobara,M. et al. (2013) : Vet J. 198, 271-274.
- Frost, D., Miettinen, M. et al. (2003) : Vet Pathol. 40, 42-54
- Isotani, M., Bonkobara,M. et al. (2010) : Br J Haematol. 148, 144-153
★変異の検出
点変異は主に、確実性と検査コストの抑制を意識して設計された独自のプライマーを使用し、変異ごとにPCR-RFLP 法*またはアリル特異的PCR*で解析します。
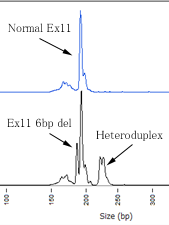
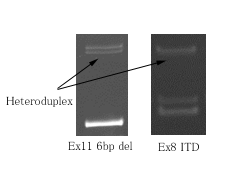
欠失挿入変異の検出にもPCR-RFLP 法等が使われますが、ヘテロデュプレックス由来のシグナルもエキストラバンドとして検出され、判定の補助に役立ちます。
- *PCR-RFLP 法・・・・・・PCR 産物を制限酵素処理して得られる断片長の違いを利用して変異の有無を判定する方法
- *アリル特異的PCR法・・・変異アリルに特異的なプライマーを用いる高感度な変異検出法
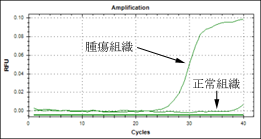
★パラフィン切片からの遺伝子検査

遺伝子検査にはホルマリンによる処理がなされていない新鮮組織が最も適していますが、病理検査用のパラフィンブロックがある場合、未染色のパラフィン切片からDNA を抽出することも可能です。
パラフィン切片を用いる遺伝子検査では、別途おこなわれる組織検査で腫瘍部位を確認し、その部分だけを掻き取ることで腫瘍の割合の高い試料を準備できるメリットがあります。カホテクノではパラフィン切片からの高い解析成功率(99.5%)を実現しています。
- DNA へのダメージはサンプルの固定条件、保存条件によって異なります。
- DNA へのダメージを最小にするため、固定には中性緩衝ホルマリン溶液の使用が推奨します。